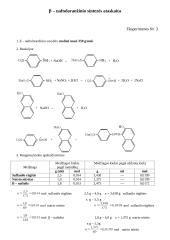
Pristatymai
Fermentai, fermentinės reakcijos
• • FERMENTAI • Fermentai (enzimai E) – tai biologinėse sistemose vykstančių reakcijų katalizatoriai • Junginys, veikiamas fermento, vadinamas substratu (S) • Po fermentinės reakcijos susidaręs junginys, vadinamas produktu (P) • Kompleksas, susidarantis reakcijos metu tarp fermento ir substrato, vadinamas fermento-substrato kompleksu (ES) • • Katalitinės fermentų savybės • Didina reakcijos greitį • Reakcijos metu fermentai nesunaudojami • Didina tiek tiesioginės, tiek grįžtamosios reakcijos greitį, t.y. neveikia katalizuojamos reakcijos pusiausvyros konstantos • Veikia tik termodinamiškai palankias reakcijas • Didelis katalitinis pajėgumas (pvz., karboanhidrazė greitina reakciją 107 kartų) • Specifiškumas (veikia tik tam tikrus substratus ar reakcijos tipus) • Veikimas švelniose sąlygose (pH, temperatūra, slėgis) • Fermentų aktyvumas yra reguliuojamas • Fermentų klasifikacija • • • • • Nr. • • Klasifikacija • • Biocheminės savybės • • 1. • • Oksidoreduktazės • AH + B ↔ A + BH • • Katalizuoja oksidacijos-redukcijos (elektronų pernešimo) reakcijas. • • 2. • • Transferazės • A-B + C ↔A + B-C • • Perneša funkcines grupes tarp donoro ir akceptoriaus molekulių • • 3. • • Hidrolazės • A-B + H2O ↔ A-H + B-OH • • Katalizuoja įvairių junginių hidrolitinio skilimo reakcijas (prijungiant vandenį). • • 4. • • Liazės • X Y • A-B ↔A=B + X-Y, • X-Y = H2O, H2S, NH3, CO2 • • Katalizuoja įvairių atomų grupių grįžtamąjį prisijungimą prie junginių, kuriuose yra dvigubasis ryšys. • • 5. • • Isomerazės • X Y Y X • A-B ↔ A-B • • Vienus izomerus paverčia kitais (L – D isomerizacija ir pan.). • • 6. • • Ligazės • A+B ↔ A-B • • Katalizuoja kovalentinio ryšio susidarymą tarp dviejų junginių • • Fermentų klasifikacija pagal jų sudėtį: • Fermentai, sudaryti tik iš aminorūgščių – paprastieji fermentai • Fermentai, sudaryti iš nebaltyminės dalies ir baltymo - sudėtiniai fermentai • Baltyminė fermento dalis – apofermentas • Nebaltyminė fermento dalis – kofaktorius • Organinės kilmės kofaktoriai – kofermentai • Sudėtiniai fermentai dar žinomi kaip holofermentai • Apofermentas+ kofaktorius = holofermentas • • Kofaktoriai tai: • Mažos neorganinės molekulės, pvz., metalų jonai • Organinės molekulės - kofermentai • Kai tarp apofermento ir kofermento nesusidaro stiprus ryšys, organinė molekulė vadinama kofermentu • Kai tarp apofermento ir kofermento susidaro stiprus ryšys, organinė molekulė vadinama prostetine grupe • Nikotinamido Adenino Dinukleotidas (NAD+) • • • Nikotinamido Adenino Dinukleotido Fosfatas (NADP+) • • • Kofermentų vaidmuo • 1. Perneša chemines grupes nuo vienų reakcijoje dalyvaujančių junginių kitiems, pvz., NAD + (ir NADP+) (susidaro iš vitamino niacino): • NAD + yra kofermentas katabolinėse oksidacijos-redukcijos reakcijose NADP + yra kofermentas anabolinėse oksidacijos-redukcijos reakcijose • ◦ 2. Kofermentai reakcijos eigoje chemiškai pakinta, todėl jie gali būti laikomi specialia substratų grupe (arba antriniais substratais). • Kofermentų klasifikacija • Gali būti klasifikuojami pagal atliekamą funkciją, kilmę ar cheminę struktūrą: • Kofermentų klasifikacija pagal atliekamą funkciją: • Oksidacijos-redukcijos kofermentai - NAD + ,NADP+, FMN, FAD, lipo rūgštis, CoQ; • pernešantys kitas grupes kofermentai – kofermentas A (CoA), tetrahidrofolio rūgštis (THFR), piridoksalio fosfatas, tiamindifosfatas (TDP), biotinas, metilkobalaminas; • Izomerizacijos ir kitiems procesams reikalingi kofermentai, pvz., deoksiadenozilkobalaminas. • • Fermentų, kofermentų ir vitaminų tarpusavio ryšys • Fermento aktyvumo vienetai • Fermento aktyvumas nustatomas esant optimalioms reakcijos sąlygoms (pH, temperatūra (25, 30 ar 37o C), substrato perteklius matuojamas pradinis reakcijos greitis) • 1964 m. pasiūlytas tarptautinis vienetas (TV) – tai fermento kiekis, katalizuojantis 1 mikromolio substrato virtimus per minutę standartinėmis sąlygomis (mikromol/min) • 1972 įvedant SI sistemą pasiūlytas fermentų aktyvumo vienetas katalas (kat) – tai fermento kiekis, kuris katalizuoja 1 molio (1M) substrato virtimus per sekundę (mol/s) • 1 katalas = 6 x 107 TV 1 TV = 1,666 x 10-8 kat • Santykinis fermento aktyvumas – fermento aktyvumo vienetų (TV) skaičius 1 mg fermento preparato (TV/mg) • • Cheminėms reakcijoms būdinga: • Termodinamika – apibūdina reakcijos energijos balansą (G) ir pusiausvyrą Kp • Kinetika - apibūdina reakcijos greitį • Fermentai veikia tik reakcijų kinetiką, bet neveikia jų termodinamikos • A B Fermento molekulės modelis • Fermento AC yra fermento paviršiaus dalis, kurioje • vyksta substrato molekulės prijungimas ir jo cheminių • virsmų katalizė • Fermento AC sudarytas iš: ◦ Katalizės centro ◦ Surišimo centro ◦ S+E ES EP E+P ◦ Fermento AC būdinga: • AC užima labai mažą fermento dalį (apie 2-5% fermento paviršiaus) • Dauguma substratų jungiasi prie fermento AC silpnais ryšiais • Substrato prisijungimo specifiškumas priklauso nuo tikslaus atomų išsidėstymo pagal: ▪ tiesioginio atitikmens arba ▪ priverstinio atitikmens modelį • trimatė erdvinė struktūra(plyšiai) • Dažniausios AC aminorūgštys: His, Ser, Asp, Glu, Lys, arg, Cys. • Fermento-substrato sąveikos galimi modeliai: ▪ tiesioginio atitikmens (rakto-spynos) – 1894 m. pasiūlė Emilis Fišeris ▪ priverstinio atitikmens modelis– 1958 m. pasiūlė Danielis Košlandas ▪ • • Heksokinazės konformaciniai pokyčiai priijungiant substratui • Fermentų specifiškumas • Fermentai didina reakcijos greitį mažindami pereinamosios būsenos energiją (mažina reakcijos aktyvacijos laisvąją energiją) • Fermentinės katalizės mechanizmai • Skiriami 4 pagrindiniai fermentinės katalizės mechanizmai: • Substratų suartinimo ir orientacijos efektas (arba entropijos efektas). • Dvisubstratės (ir daugiau) reakcijos atveju reaguojantys substratai fermento aktyviajame centre suartinami ir tinkamai orientuojami. • Ryšių įtemptis (pereinamosios būsenos erdvinis stabilizavimas). Prisijungus fermentui prie substrato kai kurie substrato ryšių ilgiai ar valentiniai kampai nukrypsta nuo įprastinių dydžių, todėl energija, reikalinga šiems ryšiams suardyti, sumažėja. • Rūgštinė-bazinė katalizė. • Katalizėje dalyvaujančios rūgštinėmis arba bazinėmis savybėmis pasižyminčios aminorūgštys gali prisijungti arba atiduoti protonus substratui. Taip padidinamas substrato krūvis bei reaktyvumas (elektrostatinis destabilizavimas). Šis katalizės mechanizmas sutinkamas beveik visose fermentinėse reakcijose. • Kovalentinė katalizė. • Katalizės metu aktyviajame centre tarp fermento ar kofermento ir substrato susidaro kovalentinis ryšys. Suartinimo ir orientacijos efektas Ryšių įtemptis (pereinamosios būsenos erdvinis stabilizavimas) Rūgštinė-bazinė katalizė • Cheminės reakcijos greitis • Cheminės reakcijos greitis – tai reaguojančių molekulių skaičius, paverčiamas produktu per laiko vienetą • -[A] = k[B] • Produkto koncentracijos [B] padidėjimas: • [B] = k[A] • A ------> B • Substrato koncentracijos [A] sumažėjimas: • Fermentinės reakcijos greitis • Fermentų kinetika • E + S ES ES* EP E + P • • Km – tai substrato koncentracija [S], kuriai esant reakcijos greitis lygus pusei maksimalaus (1/2 Vmax) • Fermentų kinetika • • • • • • Dvigubi atvirkštiniai grafikai • Lainuiverio-Berko grafikas (1/Vo atidedama prieš 1/[S]). • • Reakcijos greičio priklausomybė nuo substrato koncentracijos [S] • • Reakcijos greičio priklausomybė nuo temperatūros • Reakcijos greičio priklausomybė nuo pH • FERMENTŲ INHIBAVIMAS • NEGRĮŽTAMASIS INHIBAVIMAS (katalitiniai nuodai) – inhibitoriai jungiasi su fermentais kovalentiniais ryšiais. • GRĮŽTAMASIS INHIBAVIMAS – inhibitoriai jungiasi su fermentais nekovalentiniais ryšiais. Sumažėjus inhibitoriaus koncentracijai, fermento aktyvumas atsistato. • Negrįžtamasis inhibavimas • Negrįžtamas kovalentinis modifikavimas, pvz., Hg jungiasi su fermente esančiomis –SH grupėmis kovalentiniais ryšiais • Pereinamosios būsenos struktūriniai analogai (fermento AC komplementarus substrato pereinamajai būsenai). • Savižudybės inaktyvikliai, dar vadinami mechanizmu pagrįsti inhibitoriai Negrįžtamasis inhibavimas • Negrįžtamasis inhibavimas • • Negrįžtamasis inhibavimas • GRĮŽTAMASIS INHIBAVIMAS • • Inhibavimo tipas • Fermento prisijungimo vieta • Kinetinis poveikis • Konkurentinis inhibavimas • Specifinė katalitinei vietai, kur inhibitorius konkuruoja su substratu. Inhibavimą pašalina substratas. • Vmax nesikeičia; • Km padidėja. • Nekonkurentinis inhibavimas • Inhibitorius jungiasi prie E ar ES komplekso ne katalitinėje vietoje. Substrato prisijungimas nekinta, bet ESI kompleksas nevirsta produktu. Inhibavimo substratas nepašalina. • Vmax sumažėja proporcingai inhibitoriaus koncentracijai; • Km nesikeičia. • Bekonkurentinis inhibavimas • Inhibitorius jungiasi tik prie ES komplekso ne katalitinėje vietoje. Substrato prisijungimas keičia fermento struktūrą, todėl prie ES komplekso gali prisijungti inhibitorius. Inhibavimo substratas nepašalina. • Vmax sumažėja; • Km padidėja Konkurentinis inhibavimas • Konkurentiniai inhibitoriai – tai struktūriniai substrato analogai, besijungiantys prie AC. • Vmax nesikeičia • Km padidėja ▪ Konkurentinis inhibavimas (kinetinių konstantų nustatymas) • • • Nekonkurentinis inhibavimas • Nekonkurentiniai inhibitoriai jungiasi kitoje vietoje nei substratas (ne AC). • Nekonkurentinio inhibitoriais jungimasis sąlygoja konformacinius fermento pokyčius, perduodamus ir aktyviajam centrui. • Vmax sumažėja proporcingai inhibitoriaus koncentracijai • Km nesikeičia. • Nekonkurentinis inhibavimas (kinetinių konstantų nustatymas) • FERMENTŲ AKTYVUMO REGULIAVIMAS • Priklausomai nuo fiziologinių poreikių: • • Keičiama fermentų koncentracija • II. Keičiamas jau esančių fermentų aktyvumas (koncentracija nesikeičia). • • Fermentų koncentracija keičiama: • 1. Fermentų sintezė reguliuojama genų raiškos (ekspresijos) lygyje; • 2. Fermentų degradavimas (priklauso nuo proteolitinių fermentų aktyvumo); • 3. Neaktyvių profermentų negrįžtamas kovalentinis modifikavimas, pvz., zimogenų aktyvinimas. • 1 ir 2 būdai yra palyginti lėti fermentų koncentracijos reguliavimo būdai (valandos, dienos). • • Tai greiti ir grįžtami fermentų reguliacijos būdai. • • Keičiamas fermentų aktyvumas: • 1. Alosterinė reguliacija; • 2. Grįžtamoji kovalentinė modifikacija (pvz., fermentus fosforilina kinazės ir defosforilina fosfatazės); • 3. Sąveika su kontrolės baltymais, pvz., kalmodulinu. • Alosterinė reguliacija • Alosterinių fermentų (allos – kitas, stereos – erdvė) aktyvumas reguliuojamas prisijungiant alosteriniams efektoriams kitoje nei aktyvusis centras vietoje. • Alosteriniai efektoriai prie fermento prisijungia nekovalentiniais ryšiais. • Alosteriniai fermentai • Pagrindinės savybės: • Fermentus sudaro 2 ir daugiau subvienetų (tai oligomeriniai baltymai) • Egzistuoja 2 fermentų konformacinės būsenos: ◦ R (angl.relaxed) – aktyvi, t.y. palanki substartui prisijungti ◦ T(angl. tense or taut) – neaktyvi, t.y. nepalanki substratui prisijungti • Konformaciniai subvienetų pokyčiai yra kooperatyvūs, t.y. perduodami vienų kitiems • Fermentams būdinga sigmoidinė (S formos) prisotinimo substratu kreivė Alosteriniai efektoriai • Neigiami alosteriniai efektoriai - mažina fermentų aktyvumą • Teigiami alosteriniai efektoriai - didina fermentų aktyvumą • Homotropiniai efektoriai – pats substratas veikia kaip alosterinis efektorius. • Heterotropiniai efektoriai – efektoriaus prigimtis yra skirtinga nei substrato (pvz., reguliavimas grįžtamuoju ryšiu produktu). • • Alosteriniai fermentai • Alosterinių efektorių prisijungimas keičia fermento aktyvumą dėl konformacijos pokyčių • • Neigiamas alosterinių inhibitorių poveikis fermento aktyvumui Alosteriniai fermentai • Nealosteriniams fermentams būdinga Alosteriniams fermentams hiperbolinė prisotinimo substratu kreivė būdinga sigmos formos prisotinimo substratu kreivė • Alosteriniai fermentai • Kovalentinis fermentų modifikavimas (grįžtamas) • Dažniausias modifikavimas – fosforilinimas. ▪ Fosforilinamos Ser, Thre ar Tyr OH grupės. Fosfato grupė turi neigiamą krūvį, todėl jos buvimas keičia fermento konformaciją. • Fermentas turi 2 konformacijas – fosforilintą ir nefosforilintą, kurių viena būna aktyvi. • Fermentą fosforilina nuo ATP priklausomos proteinkinazės; defosforilina - fosfoproteinfosfatazės • Kovalentinis fermentų modifikavimas • • • IZOFERMENTAI • Tai fermentai, katalizuojantys tą pačią reakciją, tačiau besiskiriantys fizinėmis cheminėmis savybėmis (struktūra), kinetinėmis konstantomis (Vmax ir Km)ar lokalizacija, pvz., laktato dehidrogenazė: • Pyruvate + NADH + H+ Lactate + NAD+ • Laktato dehidrogenazė sudaryta iš 2 rūšių (H –angl. Heart –dominuoja širdyje; ir M –angl._ muscle – dominuoja raumenyse ir kepenyse) 4 subvienetų: • M4, M3H, M2H2, MH3, ir H4. • Izofermento tipas priklauso nuo organo,t.y. yra organospcifinis • • Fermentų reikšmė medicinoje • Tai raktas įgimtų metabolizmo defektų supratimui • Svarbūs detoksinimo procesui • Reikšmingi ligų diagnostikai • Reikšmingi ligų gydymui ir monitoringui • Chemoterapijos taikiniai • Kryptingos vaistų paieškos taikiniai • Svarbūs metabolinei kontrolei ir balansui • • • Fermentai medicinoje Vaistai Diagnostika Vidiniai Išoriniai Fermentai kraujyje Kolagenazė Hialuronidazė Geriamieji Švirkščiamieji Funkciniai Nefunkciniai (krešėjimo) Asparaginazė Virškinimo (vėžio gydymui) Organų fermentai fermentai Streptokinazė (trombų tirpinimui) Organospecifiniai izofermentai Imobilizuoti fermentai naudojami kaip reagentai •
Šį darbą sudaro 1798 žodžiai, tikrai rasi tai, ko ieškai!
★ Klientai rekomenduoja
Šį rašto darbą rekomenduoja mūsų klientai. Ką tai reiškia?
Mūsų svetainėje pateikiama dešimtys tūkstančių skirtingų rašto darbų, kuriuos įkėlė daugybė moksleivių ir studentų su skirtingais gabumais. Būtent šis rašto darbas yra patikrintas specialistų ir rekomenduojamas kitų klientų, kurie po atsisiuntimo įvertino šį mokslo darbą teigiamai. Todėl galite būti tikri, kad šis pasirinkimas geriausias!
Norint atsisiųsti šį darbą spausk ☞ Peržiūrėti darbą mygtuką!
- Cheminių junginių pristatymas
- 54 psl., (1798 ž.)
- Skaidrės 3 MB
- Lygis: Universitetinis
Mūsų mokslo darbų bazėje yra daugybė įvairių mokslo darbų, todėl tikrai atrasi sau tinkamą!
Panašūs darbai
Kiti darbai
Privalumai
Atsisiuntei rašto darbą ir neradai jame reikalingos informacijos? Pakeisime jį kitu nemokamai.
Pirkdamas daugiau nei vieną darbą, nuo sekančių darbų gausi 25% nuolaidą.
Išsirink norimus rašto darbus ir gauk juos akimirksniu po sėkmingo apmokėjimo!
Atsiliepimai