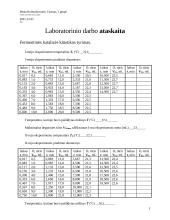
Laboratoriniai darbai
Cheminės kinetikos ir pusiausvyros tyrimas
Nr.
Greitis V=
koeficientas
1
24
113
0.009
2.22
2
34
56
0.02
Pagal lygtį apskaičiuojame reakcijos temperatūrinį koeficientą:
.
1. Katalizatoriaus įtaka reakcijos greičiui.
Į mėgintuvėlį įpilame 1-2ml 3 konc. vandenilio peroksido tirpalo ir įberiame truputį mangano dioksido. Prie išsiskyrusių dujų prikiškite rusenančią balaną. Parašome vandenilio peroksido skilimo lygtį:
MnO2 (k)
2H2O2 2H2O + O2
MnO2 atlieka katalizatoriaus vaidmenį. Šiuo atveju vyksta heterogeninė reakcija. Ji vyksta tuomet, kai reaguojančių medžiagų ir katalizatoriaus fazės yra skirtingos.
2. Koncentracijos įtaka cheminei pusiausvyrai.
Geležies chloridui reaguojant su kalio rodanidu, susidaro raudonos spalvos geležies rodanidas Fe(SCN)3. Ši reakcija grįštamoji:
FeCl3 + 3KSCN...
Šį darbą sudaro 261 žodžiai, tikrai rasi tai, ko ieškai!
★ Klientai rekomenduoja
Šį rašto darbą rekomenduoja mūsų klientai. Ką tai reiškia?
Mūsų svetainėje pateikiama dešimtys tūkstančių skirtingų rašto darbų, kuriuos įkėlė daugybė moksleivių ir studentų su skirtingais gabumais. Būtent šis rašto darbas yra patikrintas specialistų ir rekomenduojamas kitų klientų, kurie po atsisiuntimo įvertino šį mokslo darbą teigiamai. Todėl galite būti tikri, kad šis pasirinkimas geriausias!
Norint atsisiųsti šį darbą spausk ☞ Peržiūrėti darbą mygtuką!
- Chemijos laboratorinis darbas
- 2 psl., (261 ž.)
- Word failas 40 KB
- Lygis: Mokyklinis
Mūsų mokslo darbų bazėje yra daugybė įvairių mokslo darbų, todėl tikrai atrasi sau tinkamą!
Panašūs darbai
Privalumai
Atsisiuntei rašto darbą ir neradai jame reikalingos informacijos? Pakeisime jį kitu nemokamai.
Pirkdamas daugiau nei vieną darbą, nuo sekančių darbų gausi 25% nuolaidą.
Išsirink norimus rašto darbus ir gauk juos akimirksniu po sėkmingo apmokėjimo!
Atsiliepimai